DEHP expozíció
A ftalátok közé tartozó dietilhexil-ftalátot (DEHP) széles körben használják a PVC-ből (polivinil-klorid) készült orvosi eszközök (pl. vértartó zacskók, csövek, katéterek és egyszer használatos kesztyűk) lágyítására, hogy ezek az eszközök hajlékonyabbá és jobban használhatóbbá váljanak. A legújabb kutatások alapján a ftalátokkal kapcsolatos kitettség teratogén vagy karcinogén következményekkel járhat vagy reprodukciós toxicitást okozhat, ezért alternatív anyagokat fejlesztettek ki a PVC eszközök lágyítására és rugalmasabbá tételére.
A dietilhexil-ftalát (DEHP) mellett a leggyakrabban használt plaszticizálók a ftalátok, leginkább az alábbiak:
- DIDP (di-izodecil-ftalát)
- DINP (di-izononil-ftalát)
- DBP (dibutil-ftalát)
- BBP (butilbenzil-ftalát)
A ftalátok mellett nem ftalát típusú anyagok is forgalomban vannak, bár azok jelenlegi piaci aránya csak 8–10%. Ezek az adipátok, a citrátok, a foszfátok, a trimellitátok stb.
A PVC és a plaszticizálók
A polivinil-kloridot (PVC-t) a mindennapi életben használt számos használati cikk, például játékok, építőanyagok, például padlóburkolók, kábelek, valamint egészségügyi termékek gyártása során felhasználják.1 A nem plaszticizált PVC szobahőmérsékleten kemény és törékeny. Emiatt szükség van a plaszticizálókra a polimer rugalmasságának növeléséhez. A plaszticizálók adalékanyagok, leggyakrabban ftalát észterek, amelyek beágyazódnak a polimerláncok közé, szétnyomva azokat, ezáltal lágyítva az anyagokat. A PVC-hez hasonló műanyagok esetén minél több plaszticizálót adnak hozzájuk, annál rugalmasabbak és tartósabbak lesznek (lásd 1. ábra, Az anyagok átlagos PVC-tartalma).2
Common alternatives include TOTM and Hexamoll DINCH, as well as the newly developed DEHT/DOTP (DEHT = Di(2-ethylhexyl) terephthalate resp. DOTP = Dioctyl terephthalate).
A PVC-hez számos plaszticizálót használnak. A PVC-ből készült orvosi eszközökhöz használt plaszticizáló a DEHP.3
A rugalmas polimer anyagok DEHP tartalma széles tartományban változik, legtöbbször 30–35% között van (w/w). Ezzel ellentétben a polietilén és a polipropilén nem tartalmaz plaszticizálót.4,5
DEHP
A DEHP a természetben nem fordul elő.
Az elmúlt évtizedekben a DEHP előállítás világszerte nőtt. A PVC a polietilén után a második legnagyobb mennyiségben előállított nyersanyag, jelenleg évente több, mint 18 tonnát állítanak elő belőle (a világ szintű felhasználást lásd a 3. ábrán). A PVC előállításának kémiai folyamata három lépésből áll: első a monomer, a vinil-klorid előállítása, második a monomer egységek összekapcsolása a polimerizációs eljárás során, majd a polimer elegyítése az adalékanyagokkal.6
A DEHP ipari és késztermékként való felhasználása három fő termékcsoportra osztható1:
I) PVC
II) nem PVC polimerek
III) nem polimerek
A DEHP körülbelül 97%-át polimerek, főként a PVC plaszticizálásához használják fel.
Néhány rugalmas, PVC-ből készült, DEHP-t tartalmazó késztermék:
- Kábelek és drótok szigetelése
- Profilok és csövek
- Lemezek, filmek, fal- és tetőfedés, padlóburkolók
- Bevonatok és műbőr (autós ülések, otthoni bútor), cipők és csizmák, outdoor és esővédő viselet
- Tömítő- és szigetelőpaszták, Plastisols, pl. alvázvédő anyagok
- Játékok és gyermekgondozási cikkek (cumik, rágókák, összenyomható gumijátékok, kiságy bélelő párnák stb.)
- Egészségügyi termékek
A DEHP-t és más plaszticizálókat adalékanyagként alkalmazzák gumikhoz, latexhez, ragasztómézgához és tömítőanyagokhoz, tintákhoz és pigmentekhez, valamint kenőanyagokhoz.1
Néhány nem polimer anyagből készült, DEHP-t tartalmazó késztermék:
- Lakkok és festékek
- Ragasztók és tömőanyagok
- Nyomtatókhoz való tinták
- ielektrikus folyadékok és kondenzátorok
- Kerámiák
PVC és DEHP az egészségügyi termékekben
Az orvosi eszközök gyártása során felhasznált PVC csak tört része a PVC éves előállítási mennyiségének. Ennek ellenére azonban a plaszticizált PVC orvosi eszközökben történő széleskörű felhasználása számos okból nagyon fontos7:
- Széles termékpaletta – a csövektől a membránokig – rugalmasságának biztosítása
- Kémiai stabilitás és sterilizálhatóság
- Olcsó és széles körben elérhető
- Nincs bizonyíték a betegre nézve jelentős káros következmények tekintetében
Európában évente körülbelül 3×104 tonna plaszticitált PVC-t használnak fel orvosi célra7, infúziós és vértranszfúziós zsákok, infúziós csövek, enterális és paranterális tápláláshoz való zsákok és csövek, valamint cardiopulmonalis bypasshoz és extracorporalis membrán oxigenizációhoz való eszközök előállításához.
Tudta?

(1) SCENIHR Opinion on the safety of medical devices containing DEHP plasticized PVC or other plasticizers on neonates and other groups possibly at risk (2008).
Okai
A DEHP-tartalmú PVC-ből készült infúziós folyadéktartályok esetében az alábbi három fő tényező ad aggodalomra okot:
DEHP-kioldódás
A mindennapi életben mindenki ki van téve kis mennyiségű DEHP hatásának. Néhányan azonban nagy mennyiségű DEHP hatásának is ki lehetnek téve bizonyos egészségügyi beavatkozások következtében. A DEHP kioldódhat a műanyag orvostechnikai eszközökből a műanyaggal kontaktusba kerülő oldatokba.
A kioldódó DEHP mennyisége függ a hőmérséklettől, a folyadék lipidtartalmától és a műanyaggal való érintkezés időtartamától. A súlyos betegek gyakran igényelnek egynél több ilyen beavatkozást, így ők még nagyobb mennyiségű DEHP-vel érintkeznek.17
A DEHP egy átlagos vértranszfúziós zsák tömegének 30–40%-át teheti ki.18 Jaeger és Rubin beszámoltak arról, hogy a PVC anyagú vértranszfúziós zsákokból felszabaduló DEHP bejutott a véralkotórészekbe; adataik szerint a felszabadulás sebessége 4 °C-on tárolt teljes vér esetén 0,25 mg DEHP/100 ml/nap volt. Felnőtteknek adott vértranszfúzió esetén 600 mg-os DEHP-expozícióról számoltak be.19
A vértranszfúziós zsákokban tárolt thrombocyta szuszpenzió esetén a felszabaduló DEHP mennyisége mérhető volt a thrombocytákban. Becslések alapján egy beteg összesen 26,4–82,4 mg DEHP-t kapott öt zsák beadása esetén.18
Mivel a thrombocyta infúzió általában 30 percig tart, időben egyenletes DEHP felszabadulási sebességet feltételezve a thrombocyta beadáshoz használt cső legfeljebb 1,0 mg-mal járulhat hozzá az összmennyiséghez, ami elhanyagolható.21
Más szerzők jelentős mennyiségű DEHP felszabadulásról számoltak be a PVC-ből készült infúziós zsákok, például parenterális táplálásra szolgáló oldatok22, citosztatikumok15 vagy antibiotikumok.23,24
A szorpció egy fizikai és kémiai folyamat, amelynek során az egyik anyag kötődik a másikhoz.
A szorpció speciális esetei:
- Kioldódás – A zsák falának anyagai bejutnak az oldatba15
- Adszorpció – Az oldatban lévő gyógyszer, pl. Diazepam16, kötődik a zsák belső falához
- Abszorpció – Az oldatban lévő gyógyszer, pl. izoszorbid-dinitrát bejut a zsák falába25
Környezeti expozíció
A környezet szempontjából két szempontot kell figyelembe venni: Az egyik a termék élettartama során a műanyagból felszabaduló DEHP mennyisége, a másik a PVC előállítása és megsemmisítése során képződő melléktermékek.
A DEHP felszabadulása a környezetbe
A nagy mennyiségű DEHP-tartalmú polimerek az alábbiak szerint halmozódnak fel:
- Hosszú használati idejű késztermékek (pl. alapanyagok)
- Szeméttárolók
- A környezetben maradó hulladék (polimerdarabok)
- A DEHP addig marad stabil, amíg a molekula a polimer mátrixban marad. A nagy stabilitás miatt a DEHP mennyisége a technoszférában (beleértve a hulladékot is) még mindig nő. A DEHP teljes megoszlása 2% a levegőben, 21% a vízben és 77% a kommunális/ipari hulladékban.1
A PVC gyártása és megsemmisítése során keletkező melléktermékek
A PVC gyártása és különösen égetése során számos toxikus melléktermék szabadul fel a környezetbe: A poliklorinált-dibenzodioxinok (PCDD-k), a polikarbonált-dibenzofuránok (PCDF-ek) és a dioxin-szerű poliklorinált-bifenilek (PCB-k) strukturálisan rokon kémiai vegyületek, amelyek nem bomlanak le a környezetben, és bioakkumulálódhatnak állati élelmiszerforrásokban és a humán szövetekben.30 Féléletidejük a szervezetben becslések szerint hét–tizenegy év.31
Például: Ciprofloxacin
A Cipro® IV (Bayer AG, INN: ciprofloxacin) címkeszövegében szerepel, hogy a gyógyszer PVC tartályából DEHP szabadulhat fel legfeljebb 5 ppm (részecske per millió) koncentrációban. A gyógyszerrel a betegbe jutott DEHP adag megbecsülhető a gyógyszert tartalmazó oldat térfogata és a beadási gyakoriság alapján. Enyhe húgyúti fertőzések esetén a ciprofloxacin javasolt adagja 12 óránként 200 mg. A gyógyszer 100 ml oldatban 200 mg gyógyszert tartalmazó rugalmas PVC tartályban kerül forgalomba. Ha a DEHP koncentráció az oldatban 5 ppm vagy 5 mg/l, akkor a húgyúti fertőzés miatt kezelt betegbe jutó DEHP mennyisége az alábbiak szerint alakul: 5 mg DEHP/l × 100 ml/ alkalmazás × 2 alkalmazás /nap × 0,001 l/ml = 1 mg DEHP/ nap. Súlyosabb fertőzések esetén agresszívebb kezelésre van szükség. Például a súlyos légúti, csont-, ízületi vagy bőrfertőzések esetén a ciprofloxacin adagja 8 óránként 400 mg. Ezen adagolási séma esetén a bejutott DEHP mennyisége a következőképpen alakulna:
5 mg DEHP/l × 200 ml/alkalmazás × 3 alkalmazás /nap × 0,001 l/ml = 3 mg DEHP/nap.
Több gyógyszer beadása
Gyakran kerül sor egy infúzióban több gyógyszer beadására. Ilyen például a kinin és a multivitamin készítmények egyidejű beadása. Kimutatták, hogy a csak kinin oldatot tartalmazó PVC zsákokból kis mennyiségű DEHP szabadul fel; azonban a lipofil multivitamin koktél jelenléte drámaian megemeli a zsák falából felszabaduló DEHP menniységét. A kinin/multivitamin kombináció 48 órán keresztül 45 °C-on történő tárolását követően a DEHP koncentrációja a zsákokban elérte a 21 mg/ml-t. Ennek alapján egy 500 ml-es kinin és multivitamin koktél infúziót kapó beteg 10,8 mg DEHP-t kapna. Nem PVC-ből készült zsákok is kaphatók azokhoz a gyógyszerekhez, amelyek szolubilizációjához lipofil vivőanyag szükséges. A nem PVC-ből készült zsákokból várhatóan nem szabadul fel DEHP. Ezzel összhangban egy polietilén tartályban 15 napig tárolt paklitaxel oldatban nem volt kimutatható a DEHP.17
Egészségügyi következmények
A ftalát plaszticizálók káros egészségügyi hatásai jelenleg a média, a törvényi szabályozás és a tudományos viták tárgyát képezik. A tudomány és az ipar folyamatosan együttműködik annak érdekében, hogy kivizsgálják az aggályokat és elvégezzék a szükséges kutatásokat, ami miatt a ftalátok mára a legtöbbet vizsgált és legjobban ismert vegyi anyagokká váltak.32
Consequences of Leaching of DEHP
A DEHP negatív hatásai az emberi szervezetre
A DEHP negatív hatásai az emberi szervezetre Számos vizsgálat során kimutatták, hogy a ftalát típusú kémiai vegyületek és különösen a DEHP patkányokban károsítja a here tesztoszterontermelését. A legfrissebb kutatások bizonyítékkal szolgáltak arra, hogy a DEHP képes gátolni a felnőtt emberi szervezetben a tesztoszterontermelést.33
Ezen kívül is beszámoltak a reprodukciós rendszerre gyakorolt nemkívánatos hatásokról, például az ondó csökkent minőségéről és a férfi nemi szervek megváltozott fejlődéséről is.34
Ezt alátámasztja, hogy emlős modellekben számos ftalátot antiandrogén hatású, az endokrin rendszer működését károsító vegyi anyagként azonosítottak.35
Az endokrin rendszer működését károsító vegyi anyagok képesek megváltoztatni a hormonális szignálokat, ami a reprodukciós rendszerre, az idegrendszerre, az anyagcserére gyakorolt hatásokkal, illetve rákos megbetegedés kialakulásával járhat.35
A DEHP-expozíció súlyos veszélyeket jelent a beteg újszülöttekre és csecsemőkre nézve.36 Az intenzív osztályokon fekvő éretlen újszülöttek, akik számos orvosi beavatkozásnak vannak kitéve, a testtömegükre vetítve még nagyobb DEHP-expozíciónak lehetnek kitéve, mint a felnőttek. Ez az expozíció még azt az adagot is meghaladhatja, amely esetén állatokban reprodukciós toxicitást figyeltek meg.37
A magzati fejlődésre gyakorolt negatív hatások
Állatkísérletek során kimutatták, hogy a DEHP különösen káros a fejlődő magzatra, károsítja a reprodukciós rendszert, és here elváltozásokat okoz.33,34

7. ábra: A „National Toxicology Program” (Nemzeti Toxikológiai Program) következtetése a DEHP az emberi fejlődésre és reprodukcióra gyakorolt esetleges káros hatásaira vonatkozóan.41
A terhesség alatt nagy mennyiségű ftalátnak kitett nőknél nő a nemi szervek rendellenességével (hypospadiasissal és cryptorchismussal), született fiúgyermek születésének kockázata, illetve később gyakoribb lehet az alacsony spermiumszám és a hererák kialakulása.34,38
A DEHP karcinogenitása
Kimutatták, hogy a DEHP patkányokban és egerekben májrákot okoz és ennek indukciós módjait is alaposan kivizsgálták.39 A tüdőt, a szívet és a vesét érintő egyéb nemkívánatos hatásokról is beszámoltak.40 A WHO intézménye, a Nemzetközi Rákkutató Ügynökség (International Agency for Research on Cancer, IARC) a DEHP-t esetlegesen humán karcinogénnek (2B csoport) nyilvánította39,és ezt a véleményt számos más szerv is osztja, például az Amerikai Egyesült Államok Egészségügyi és Humán Szolgáltatási Minisztériuma.41
Az IARC a DEHP-t 2000-ben alsóbb osztályba sorolta, azonban az orvosi tudományos társadalomban jelentős kritika fogadta ezt a lépést, arra hivatkozva, hogy az IARC jelentős kutatásokat nem vett figyelembe.
A lipofil anyagok a legnagyobb aggodalomra okot adó anyagok
A DEHP bediffundál a lipofil szövetekbe és folyadékokba és így eloszlik a szervezetben, függetlenül a bejutás - orális, parenterális, inhalációs vagy dermális - módjától. Ezért sok szerző javasolja a PVC tartályok helyett polietilén vagy polipropilén tartályok használatát15, és egyre több gyógyszergyártó használ alternatív anyagokat a PVC zsák helyett a gyógyszerek, pl. a paklitaxel vagy a temszirolimusz tárolásához.
A DEHP thrombogenitása
Jól ismert, hogy a PVC anyagok thrombogenikus hatással rendelkeznek, és számottevő bizonyíték van arra, hogy a thrombocyta aggregációt az anyagban található DEHP okozza, és nem maga a PVC. Emellett a komplement rendszer aktiválódása – a nemkívánatos hematológiai hatásokkal járó folyamat beindulása – nagyobb mértékű, ha a vér DEHP-vel plaszticizált PVC-vel érintkezik, mintha más polimerrel. E hatások mindegyike káros klinikai következményeket okoz a betegekben.43,44
A DEHP-expozícióval kapcsolatos peritonealis sclerosis
A peritonealis sclerosis a peritonealis dialíziskezelés egyik súlyos szövődménye. Úgy tűnik, hogy más tényezők mellett a DEHP is szerepet játszik ennek az állapotnak a patogenezisében. A kutatási eredmények arra utalnak, hogy a DEHP szintje a DEHP tartalmú zsákokban tárolt dialízisfolyadékban elegendő a peritonealis sclerosis folyamat beindításához és a sclerosis kialakulásához.
A peritonealis sclerosis klinikai jelentőségét nem lehet alábecsülni, mivel a csökkent peritonális dialíziskapacitással rendelkező betegeket hemodialízisre kell átállítani.17
A PVC szorpciójának következményei
A gyógyszerek PVC-vel kapcsolatos szorpciója és a kezelés következményei
Míg a plaszticizálók felszabadulásának tárgyalása a gyógyszer csomagolásának toxikológiai jellemzőire fókuszált, a gyógyszerformula összetevőinek szorpciója (abszorpciója vagy adszorpciója) esetén a hatóanyag adagolásán van a hangsúly, mivel a szorpció következtében alacsonyabb dózisok beadására kerülhet sor. Ezért a szorpció befolyásolja a kezelés hatékonyságát és sikerét.27
A 6. ábrán látható a PVC-vel inkompatibilis gyógyszerek listája. Ezeket a példákat és javasolt felhasználásukat tekintve az elképzelhető következmények az anyagok jelentős aluldozírozásának következményei:
- A glioblastoma (agytumor) kemoterápiájában alkalmazott szer, a karmusztin aluldozírozása a kezelés hatástalanságához, és ezáltal a rákos megbetegedés progressziójához vezethet
- A heparin és warfarin nevű antikoagulánsok aluldozírozása vérrögképződéshez és/vagy tüdőembóliához vezethet
- A tiopentál, egy gyors és rövid hatású barbiturát típusú általános anesztetikum aluldozírozása a beteg nemkívánatos éberségéhez vezethet
- Az izoszorbid-dinitrát és a nitroglicerin, angina pectoris esetén használt dilatálószerek aluldozírozás esetén hatástalanok lehetnek, és szívinfarktus alakulhat ki.
- A nyugtatók és szorongásoldók közé tartozó klórdiazepoxid és diazepam aluldozírozása esetén nem alakul ki a kívánt hatás.
Amennyiben a szorpció hatása ismert a felhasználó számára, és emiatt a belekevert gyógyszer mennyiségét növelik, akkor ezzel számottevő megelőzhető költség takarítható meg a szolgáltató és a költségviselő számára.
A környezeti expozíció következményei
A környezetbe felszabaduló DEHP hatásai megegyeznek a fentiekben leírtakkal: a táplálékláncban akkumulálódnak, és bejutnak az emberi szervezetbe. Ennek eredményeképpen endokrin zavar, rákos megbetegedés és számos egyéb rendellenesség és betegség alakulhat ki.
Kimutatták, hogy a PVC gyártása és égetése során a környezetbe kerülő dioxinok és furánok számos toxikus hatással rendelkeznek, például dermális toxicitást, idegrendszeri fejlődési deficitet, immunotoxicitást, a reprodukciós rendszerre gyakorolt hatásokat és teratogenitást, endokrin zavart, metabolikus szindrómát és karcinogenitást okoznak.30
1997-ben a Nemzetközi rákkutató ügynökség (International Agency for Research on Cancer) a TCDD-t (2,3,7,8-tetraklorodibenzop-dioxint) a csoport legtoxikusabb összetevőjének, azaz az I. csoportba tartozó (megfelelő mennyiségű karcinogenitást igazoló bizonyítékkal rendelkező) karcinogénként határozta meg45 és a korábbi és új bizonyítékok legfrissebb áttekintése is igazolta az osztályozás helyességét.46
A fenti (Okok) című részben leírtaknak megfelelően az építőanyagokból, hulladékból és szemétlerakókból származó DEHP mennyisége továbbra is nő a levegőben, a földben és a vízben. Ez a környezeti expozíció hozzáadódik az ételből, az orvostechnikai és más eszközökből származó expozícióhoz, és ezáltal a leírt kockázatokhoz.
A PVC termelése és lebontása során felszabaduló dioxinok, furánok, toxikus melléktermékek (pl. PCDD-k, PCDF-ek és PCB-k) felezési ideje nagyon hosszú. Koncentrációjuk a táplálékláncon való felfelé haladás során egyre nő, főként a zsírszövetben. A DEHP bevitel középértéke az egyes korcsoportokban a 8. ábrán látható.
A dioxinok és a furánok a tudomány által ismert legmérgezőbb vegyi anyagok közé tartoznak. Nagymennyiségű dioxin emberben rövid idő alatt bőrelváltozásokat, például klóraknét és a bőr foltos sötét elszíneződését, valamint a májműködés megváltozását okozhatja. A tartós expozíció az immunrendszer, a fejlődő idegrendszer, az endokrin rendszer és a reproduktív funkciók károsodását okozza.
Állatok krónikus dioxin-expozíciója számos típusú rákos megbetegedést okozott. A TCDD-t a WHO Nemzetközi Rákkutató Ügynöksége (IARC) vizsgálta 1997-ben.<sup>54</sup> Állatkísérletes és humán epidemiológiai adatok alapján az IARC a TCDD-t az „ismert humán karcinogén” osztályba sorolta.
A dioxinok és a furánok egészségügyi hatásait intenzíven dokumentálták epidemiológiai és toxikológiai vizsgálatok keretében.48 Ezen kívül számos jelentős szövődmény vált ismertté súlyos balesetek, például az olaszországi sevesói katasztrófa (1976) következtében. Ennek alkalmával egy toxikus vegyi anyagokat, például 2,3,7,8-tetraklorodibenzop-dioxint vagy TCDD-t tartalmazó gőzfelhő jutott a levegőbe, amelynek következtében a kontamináció 15 négyzetkilométernyi területet és 37 000 embert érintett.
Gazdasági következmények
Az emberekre, különösen a fejlődő gyermekekre nézve a DEHP-nek jelentős egészségügyi következményei lehetnek, ahogy a fenti ábrán is látható. Ezek a zavarok jelentős gazdasági következményekkel járhatnak, súlyosabb betegségekkel melyek nagy gazdasági teherhez vezetnek.
A potenciális kockázatokkal kapcsolatos költségek
As an example, some of the health consequences to DEHP have been selected and their additional treatment costs according to reports from the current literature are displayed below (see Fig. 9). These figures only take into account pure costs for treatment. Not included are any overall economic effects such as loss of labour, gross domestic product, joblessness, etc.
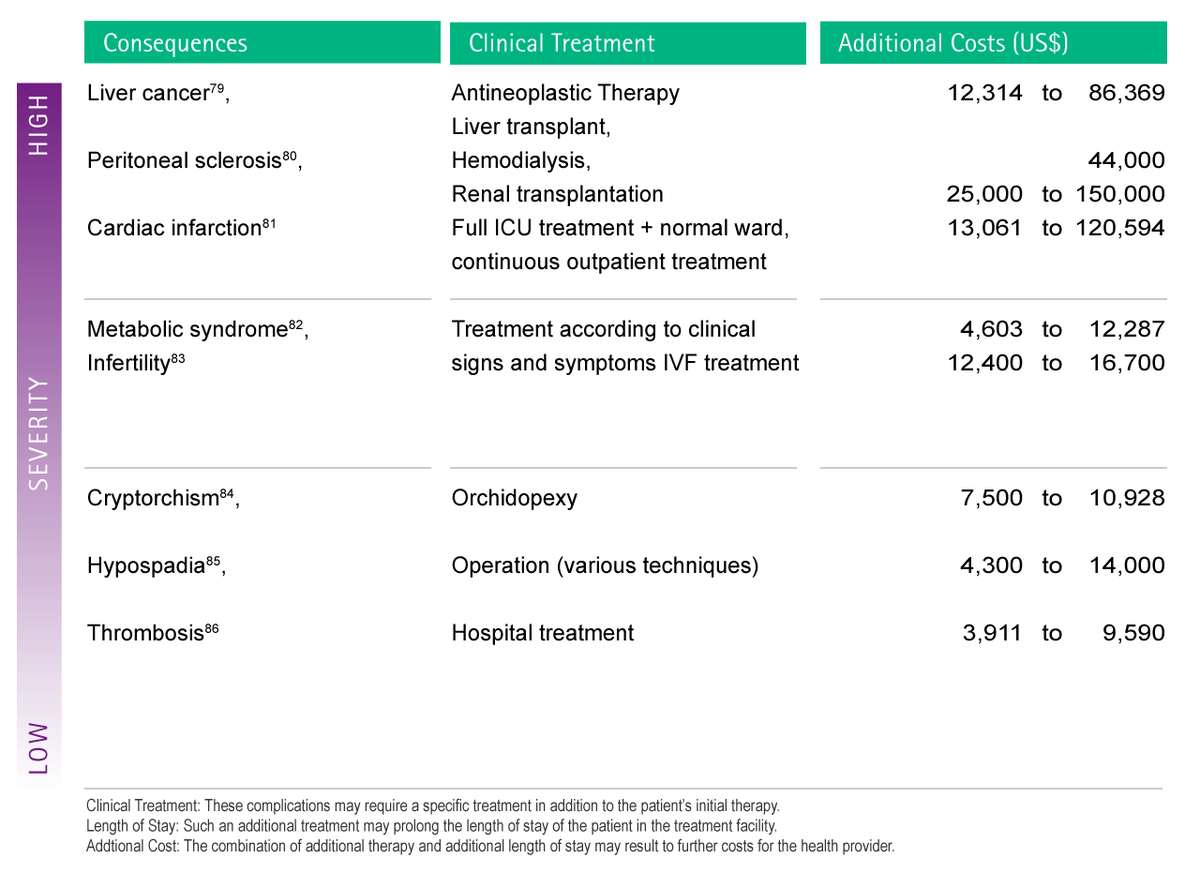
9. ábra: A DEHP-expozíció által okozott szövődmények miatt fellépő lehetséges járulékos költségek becslése. Az egyes szövődmények költségszámításhoz történő besorolásának megkönnyítése érdekében súlyossági fokozatokat vezettünk be.79,80,81,82,83,84,85,86
Megelőzés
A korábbi szakaszokban foglaltaknak megfelelően konszenzus van abban a tekintetben, hogy a DEHP plaszticizáló használata aggályos, és a tudományos fórumok világszerte javasolják használatának korlátozását. 1,4,7,17,49,50 Ezen kívül napjainkban számos alternatíva rendelkezésre áll, vagy más plaszticizálóval előállított PVC vagy teljesen új, PVC-mentes anyagok használata. Ennek következtében számos nemzetközi, országos és regionális, részben törvénybe iktatott lépés történt az egészségügyi szektorban, valamint számos más iparágban, például a játék-, élelmiszer- és italgyártásban.
Törvényi szabályozás és irányelvek
- A 143/2011-es EU szabályozásban a bisz(2-etilhexil)-ftalátot (DEHP-t) a reprodukciós rendszerre nézve toxikusna nyilvánították. 2015. január 21-től a DEHP forgalomba helyezéséhez és használatához külön speciális engedélyre lesz szükség.53
- Az Európai Unió a DEHP-PVC helyett más anyagok használatát javasolja az orvostechnikai eszközök gyártásához.51
- Az EC 1907/2006 Európai Közösségi irányelv, a „REACH” („Vegyi anyagok regisztrálása, értékelése, engedélyezése és korlátozása”, Registration, Evaluation, Authorisation and Restriction of Chemical substances) 2007. június 1-én lépett hatályba. Ebben a DEHP-t a nagyon veszélyes anyagok közé sorolták. Az ilyen anyagok használatát a helsinki Európai Vegyianyag Ügynökséggel (European Chemicals Agency, ECHA) engedélyeztetni kell.54
- A 2007/47 EC irányelvnek megfelelően a DEHP-tartalmú orvosi eszközök címkéjén fel kell tünteni ezt az információt.55
- Az Amerikai Egyesült Államok kongresszusa aláírta a 2008 augusztusában hatályba lépett Consumer Product Safety Improvement Actot (CPSIA, a biztonságos fogyasztási cikkek fejlesztéséről szóló törvényt), amelynek 108. cikkelye kimondja, hogy 2009. február 10-től törvényellenes a 0,1%-nál több DEHP-t, DBP-t vagy BBP-t tartalmazó gyermekjátékok vagy gyermekgondozási cikkek eladásra, eladási céllal, kereskedelmi forgalmazásra vagy importálásra történő gyártása.
- 2010 januárjában az ausztráliai kereskedelmi miniszter, Craig Emerson a reprodukcióra kifejtett káros hatásai miatt betiltotta a több mint 1% DEHP-t tartalmazó termékeket.56
- Az ételek csomagolására nézve a DEHP használatát az ételekkel érintkező műanyagokban és termékekben már a 2007. március 30-án életbe lépő 2007/19/EC bizottsági irányelvben betiltották. A 85/572/EEC bizottsági irányelvben meghatározták azoknak a szimuláló anyagoknak a listáját, amelyek alkalmasak a műanyagokból és az étellel érintkező anyagokból kivándorló összetevők tesztelésére.
- Ételek csomagolására a DEHP-t tartalmazó, illetve nem tartalmazó PVC csomagolóanyagok használata számos országban be van tiltva, illetve korlátozva van, például Kanadában, Spanyolországban, Dél-Kóreában és Csehországban.57
- A Német Szövetségi Gyógyszerészeti és Orvostechnikai Intézet (Bundesinstitut für Arzneimittel und Medizinprodukte – BfArM) a DEHP lágyítót tartalmazó PVC-ből készült orvostechnikai eszközök helyett alternatív termékek haszálatát javasolja éretlen csecsemők és újszülöttek esetében. A BfArM arra is felszólítja az orvostechnikai eszközök gyártóit, hogy a termékek címkéjén tüntessék fel annak DEHP-tartalmát, és helyezzenek nagyobb hangsúlyt biztonságosabb termékek kifejlesztésére.58
- Ehhez hasonlóan az Amerikai Egyesült Államok Élelmiszer és Gyógyszerhivatala (US Food and Drug Administration, FDA) kiadott egy biztonsági értékelést és egy közegészségügyi értesítést, amelyben felszólítja az egészségügyi szolgáltatókat arra, hogy bizonyos sérülékeny betegek esetén a DEHP-tartalmú termékek helyett alternatív termékeket alkalmazzanak.17
- Többek között a Health Canada tudományos szakértői testülete a DEHP vonatkozásában azt javasolja, hogy a lipofil gyógyszerek tároló zsákjai ne tartalmazzanak DEHP-t<sup>65</sup>. Emellett a Health Canada javasolta a három éven aluli gyermekeknek szánt játékok és a szájba vehető, DEHP-t tartalmazó termékek értékesítésének, reklámozásának és importjának betiltását.59
- Argentína, Ausztria, Ciprus, Csehország, Dánia, Fidzsi-szigetek, Finnország, Németország, Görögország, Olaszország, Japán, Mexikó, Norvégia és Svédország betiltották a ftalátok gyermekjátékokban történő alkalmazását.52
- A 2002/95/EG (RohS, elektromos és elektronikus berendezésekben található meghatározott veszélyes anyagok használatának korlátozásáról szóló) irányelv legfrissebb változatában az Európai Unió felvette a tiltott anyagok listájára a DEHP-t.
- 2005. április 1-től az EU fogyasztói számára nem szállíthatók DEHP-t tartalmazó kozmetikai termékek a 2004. szeptember 21-én kelt – a kozmetikumok használatára vonatkozó 76/768/EEC tanácsi irányelv helyettesítésére szolgáló – 2004/93/EC bizottsági irányelvnek megfelelően.
- A környezetben tartósan fennmaradó szerves szennyezőanyagok (furánok, hexaklórbenzén és PCB-k) és dioxinok kibocsátásáról szóló Stockholmi Egyezmény előírásainak megfelelően minden félnek legalább minimálisan csökkentenie kell ezeknek az anyagoknak az emberi tevékenységek forrásából származó összkibocsátását ... később azt folyamatosan csökkenteni kell, majd, ahol az megvalósítható, teljesen meg kell szüntetni.60
- A dioxin szemétégetőben történő égetésével kapcsolatos aggályok ahhoz vezettek, hogy a Japán kormány törvénybe foglalta új tartályok és csomagolóanyagok gyártási kötelezettségét, amelyben előírta a gyártók számára, hogy a 2000. évre teljes mértékben újrahasznosítható termékeket alkalmazzanak. A törvény értelmében számos nagy japán háztartási eszköz és kozmetikum gyártónak ütemtervet kell készítenie arra vonatkozóan, hogy milyen ütemben váltanak át a polipropilén és más anyagok használatára a különböző típusú kozmetikumok, ételek és gyógyszerek csomagolásában.61
- A „Health Care Without Harm” (Ártalom nélküli egészségügyet) kampány 51 ország 420 szervezetét magába foglaló nemzetközi koalíció. A szervezetek között vannak kórházak és egészségügyi intézmények, egészségügyi szakemberek, közösségi csoportok, az egészségügy által érintett választókerületek, munkahelyi egyesületek, környezet- és egészségvédelmi szervezetek és vallási csoportok. A kampány egyik célja, hogy fokozatosan kiszorítsa a PVC és a tartós toxikus hatást jelentő vegyi anyagok használatát, és motiválja a PVC elleni kampány kiszélesítését.64
Kezdeményezések és kampányok
- 2011 novemberében az FDA (az Amerikai Egyesült Államok Élelmiszer és Gyógyszerhivatala, US Food and Drug Administration) új maximálisan megengedhető szintet (0,006 mg/l) állapított meg a palackozott víz dietilhexil-ftalát (DEHP) szintjére vonatkozóan, és a gyártók számára kötelező a DEHP szint monitorozása.62
- A Kaiser Permanente, egy amerikai egyészégügyi szolgáltató azt nyilatkozta, hogy nem értékesít több PVC-ből készült, illetve DEHP plaszticizálót tartalmazó infúziós zsákot. A szolgáltató folyamatos erőfeszítéseket tesz a kórházaiban, rendelőiben és egészségügyi intézményeiben kezelt 8,9 millió ember egészségének és biztonságának megóvása érdekében.63
- A Kaiser Permanente, a Miller Children‘s Hospital Long Beachen, a Lucile Packard Children‘s Hospital a Stanford egyetemen és a John Muir Medical Center, Walnut Creek-ben fokozatosan kivonja az újszülött intenzív osztályokon használt PVC tartalmú orvostechnikai eszközöket a használatból.64
- A Németországi Környezetért és Természetvédelemért Egyesület (Bund für Umwelt und Naturschutz Deutschland, BUND), a Károsodás Nélküli Egészségügyért (Health Care Without Harm, HCWH) és a Környezettudatos Orvoslás Eeurópai Akadémiája (European Academy for Environmental Medicine, EUROPAEM) elindította a „szennyezésmentes kórházakat” című kezdeményezést. A környezetvédelmi szervezetek felszólították a német kórházakat, hogy szüntessék be a PVC-tartalmú orvostechnikai eszközök használatát.65 A Bécsi kórházszövetséghez tartozó Glanzing gyermekklinikán működik a világon az első újszülött osztály, amely kijelentheti, hogy teljes mértékben PVC mentes műanyagokkal dolgoznak.64
- Spanyolországban több mint 60 törvényi hatóság jóváhagyta a PVC fokozatos kivonására irányuló intézkedéseket. Hasonlóan Németországban, ahol egyre több város hagyta jóvá saját nyilatkozatában, hogy a középületekben kerülni kívánják a PVC használatát.52
- Az OSPAR számos anyagot felvett az elsődleges fontosságú cselekvésre kijelölt vegyi anyagok listájára, amelyek a klór és a PVC gyártási melléktermékei vagy a PVC adalékanyagai: dioxinok és furánok, klórozott paraffinok, higany és szerves higanyvegyületek, ólom és szerves ólomvegyületek, szerves ónvegyületek és bizonyos ftalátok (DBP és DEHP).66
Kutatás és ipar
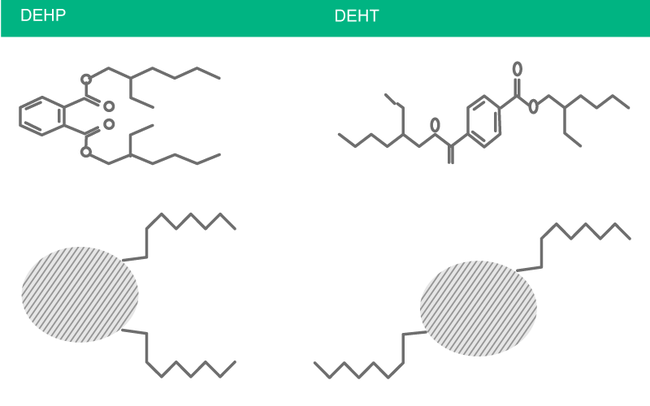
10. ábra: A DEHT-t, a dietilhexil-tereftalátot DOTP-nek (dioktiltereftalátnak) is hívják. A kémiai szerkezete nem azonos a DEHP szerkezetével.
- A B. Braun megvette és továbbfejlesztette a dietilhexil-tereftalátot (DEHT) vagy dioktil-tereftalátot (DOTP), amely egy eltérő kémiai szerkezetű ftalátmentes plaszticizáló. A PVC lágyításához a DEHT vagy DOTP az egyetlen olyan plaszticizáló, amely a tesztek során nem mutatott toxikus mellékhatásokat (lásd a 10. ábrát).7, 67
- Egyre több vegyi gyár fejleszt ki és gyárt alternatív plaszticizáló anyagokat. A plaszticizáló engedélyezése előtt átfogó és alapos vizsgálatokat kell végezni, mint például a TOTM/TEHTM és a Hexamoll® DINCH.
- Számos orvostechnikai eszköz gyártó cég, köztük a B. Braun is támogatott olyan kutatásokat, amelyekben a DEHP-PVC-t helyettesítő más anyagokat vizsgáltak orvostechnikai eszközök gyártása szempontjából.
Az alternatív plaszticizáló, a DEHT jellemzői
A dietilhexil-tereftalát (DEHT) egy általános célra szolgáló ftalátmentes plaszticizáló, amely 1975 óta van kereskedelmi forgalomban. Például a Coca-Cola és más cégek mindig is DEHT-t használtak a palackok gyártása során. A tereftalát a „T” a PET betűszóban (lásd a 20. ábrát). A játékipar is széleskörűen használja ezt a plaszticizálót.
A DEHT-t az Eastman cég fejlesztette ki és gyártotta, egyik márkaneve az Eastman 168.
A DEHT toxicitási profilja
A DEHT toxicitását széles körben vizsgálták in vitro és in vivo vizsgálatok keretében. Orális, dermális és okuláris expozícióval, valamint inhalálással végeztek akut toxicitási vizsgálatokat, amelyek során az akut, a szubakut és a szubkrónikus toxicitást vizsgálták. Minden vizsgálat során kiváló toxikológiai profilt mutattak ki.
A fejlődésre kifejtett toxicitási vizsgálatok során sem a hím patkányok szexuális differenciálódására, sem a hím nemi szervek fejlődésre kifejtett toxicitást nem mutattak ki. Ösztrogénhatást sem mutattak ki. A genotoxicitási és a mutagenitási tesztek mind negatívak voltak. A tumorok előfordulási gyakoriságára és a tumorképződésre nem gyakorol hatást, nem indukálja a máj peroxiszómáit, amit a potenciális tumorképző hatás jelének tekintenek.
Egy hím és nőstény patkányokon, a helyes laboratóriumi gyakorlatnak megfelelően végzett toxicitási vizsgálatban 4 héten keresztül adott folyamatos DEHT infúzió alkalmazását követően kimutatták, hogy az intravénás DEHT-t az állatok szisztémásan és helyileg is mellékhatások nélkül tolerálták 381,6 mg/kg/nap adagig (NOAEL=381,6 mg/kg x nap). Nem volt kimutatható hatás a DEHP-toxicitás ismert célszerveiben, a reprodukciós szövetekben/szervekben, a vesében, valamint a máj hepatocytáiban és a peroxiszómákban. A DEHT bőrirritáló képességére vonatkozóan 203 önkéntes körében végeztek klinikai vizsgálatot.68 Megállapították, hogy DEHT nem irritáló és nem indukál kontakt szenzitivitást
Ezek az adatok arra utalnak, hogy a DEHT (Eastman 168) plaszticizáló alacsony akut toxicitással rendelkezik, lényegében nem irritáló és nem valószínű, hogy kontakt szenzitivitást okoz emberben.69
A DEHT szabályozási profilja
A DEHT Eastman 168-at világszerte számos kormányhatóság alaposan megvizsgálta, és az engedélyezett anyagok listájára helyezte.
USA: A Food Contact Notification (FCN) számos élelmiszeripari alkalmazására alkalmasnak nyilvánította.70
Európai Unió: Az European Food Safety Authority (Európai Élelmiszerbiztonsági Hatóság, EFSA) jóváhagyta; az SCENIHR ellenőrizte orvosi felhasználás szempontjából. A REACH a DEHT-t nem sorolta a CMR (karcinogén, mutagén vagy reprodukciós toxicitással rendelkező) szerek közé.54 A DEHP-t nem tartalmazó termékeken fel lehet tüntetni a DEHP-mentességet megfelelő szimbólumokkal.
Németország: A Bundesinstitut für Risikobewertung (Német Kockázatfelmérő Intézet, BfR) engedélyezte a plaszticizált PVC-ben, ideértve az italos csövekben, kupakbélésként és élelmiszer csomagológanyagként történő felhasználását..
Svájc: A DEHT nem szerepel a Svájc által toxikusnak nyilvánított szerek listáján, így nem tekintendő toxikusnak.
Japán: A Japan Hygienic PVC Association (Japán PVC Higiénés Társaság) felvette a DEHT-t a pozitív listájára.
Környezeti profil
A DEHT nagyon rosszul oldódik vízben. Desztillált vízben az oldhatóság 0,4 μg/l-nek bizonyult. A vizes oldat toxicitására vonatkozóan a vízoldékonysági limit közelében lévő koncentrációval tesztelt semmilyen fajnál nem mutattak ki akut vagy krónikus hatásokat. Egy másik vizsgálat során szintén nem volt kimutatható a túlélésre gyakorolt hatás az oldékonysági határnál nagyságrendekkel nagyobb koncentráció esetén sem. Szubletális hatásokat, például a növekedésre, a reprodukcióra, a tojáshéjban történő lerakódásokra és a tojások életképességére vonatkozó káros hatásokat szintén nem észleltek a vizsgált koncentrációk esetén. Mivel a DEHT nagymértékben kötődik a vizes környezetben található üledékekhez, OECD üledék-víz kironomid toxicitási tesztet végeztek üledékkel annak kimutatása érdekében, hogy a DEHT nem befolyásolná károsan a vizes környezetben található üledékben élő organizmusokat. Az üledék teszt talapján az EC50 nagyobbnak bizonyult a módszerhez javasolt legnagyobb tesztkoncentrációnál.
A biodegradáció szempontjából a vizsgálatok kimutatták, hogy az eredeti DEHT 37–56%-a lebomlik 28 nap alatt.
E vizsgálatok alapján úgy tűnik, hogy a DEHT elsődlegesen és teljesen lebomlik.69
Orvosi eszközök és gyógyszertartályok előállításához felhasznált további anyagok
A PVC hiányosságai, különösen a kezelés hatásosságát és sikerességét befolyásoló szorpciós hatások miatt, más anyagokkal is kutatásokat végeznek orvosi eszközök és gyógyszertartályok gyártásához történő felhasználás céljából. Több inert polimer, például a polietilén-tereftalát (PET) vagy a poliamid (PA) kisebb mértékű interakciót eredményez.71,72 Másfelől nem minden polimer alkalmas gyógyszerek csomagolására. A merev mechanikai tulajdonságainak köszönhetően a PET például nehezen lenne felhasználható rugalmas csövek vagy zsákok gyártásához.27
E megfontolások miatt többrétegű fóliákat is alkalmaznak, amelyek belső rétege polipropilénből, külső rétegei polietilénből és poliészterből állnak.
A polietilén és a polipropilén szorpciós viselkedése
A polietilén (PE) és a polipropilén (PP) a poliolefinek csoportjába tartoznak. Két olyan anyagról van szó, amely megfelelőnek bizonyult az infúziós tartályok gyártásához. Az Európai Gyógyszerkönyvnek73 megfelelően az orvosi minőségű PE-ből készült gyógyszertartályok nem tartalmaznak plaszticizálót, adalékanyagot és egyéb olyan összetevőket, amelyek bejuthatnak a késztermékbe. Ezek az anyagok kémiailag inertek és nem toxikusak.
A PVC-hez jelentősen adszorbeálódó jól ismert gyógyszercsoport jellemző képviselőinek, a nitroglicerinnek és a diazepamnak a szorpciós viselkedését vizsgálták más műanyagok esetén. A PE és a PP mindkét gyógyszer esetében kisebb szorpciós arányt mutatott, mint a standard PVC csövek.27
Számos további vizsgálat kimutatta, hogy a PE/PP rendelkezik a gyógyszerek szempontjából a legalacsonyabb szorpciós potenciállal a többi műanyaghoz képest.74,75,76
Általánosságban az oldatok és a gyógyszerészeti tartályrendszerek műanyagainak interakciós tulajdonságainak modellezése alapján a PP bizonyult a legkevésbé gyógyszermegkötő tulajdonságúnak, és azt rögtön a PE követte.77
A polietilén / polipropilén környezeti hatásai
Napjainkban az egészségügyi hulladék legnagyobb részét elégetik. Például az Egyesült Királyságban a „Landfill Directive” (Szemétlerakásra vonatkozó irányelv) kimondja, hogy a klinikai hulladékot nem lehet szemétlerakóba helyezni, hanem el kell égetni. A fentiek szerint a PVC égetéssel történő hulladékártalmatlanítása során poliklorinált-dibenzo[p]-dioxinok (PCDD) és polikarbonált-dipenzo-p-furánok (PCDF) képződnek és jutnak a környezetbe füstgáz és hamu formájában.
A polietilén és a polipropilén, mint minden szénhidrogén, jól égnek. A teljes égés végtermékei a szén-dioxid és a víz, amelyek nem toxikusak és nem jelentenek környezeti kockázatot.78
Kiemelt biztonsági termékek
Tudományos bizonyíték
1 European Union Risk Assessment Report. bis(2-ethylhexyl)phthalate (DEHP)
2 Cadogan DF, Howick CJ (2000)
Plasticizers in Ullmann’s Encyclopedia of Industrial Chemistry,
Wiley-VCH, Weinheim. doi: 10.1002/14356007.a20_439.
3 Safety Assessment of Di(2-ethylhexyl)phthalate (DEHP) Released from PVC Medical Devices
http://www.fda.gov/downloads/MedicalDevices/DeviceRegulationandGuidance/GuidanceDocuments/UCM080457.pdf
4 Umweltbundesamt, Berlin, Hrsg. (2/2007)
Phthalate – die nützlichen Weichmacher mit den unerwünschten Eigenschaften: 3, 10.
5 Kroschwitz JI (1998)
Kirk-Othmer Encyclopedia of Chemical Technology.
Fourth Edition. John Wiley and Sons, New York.
6 http://www.chm.bris.ac.uk/webprojects2001/esser/manufacture.html
7 SCENIHR opinion on the safety of medical devices containing dehp plasticized pvc or other plasticizers on neonates and other groups possibly at risk 2008.
8 Haishima Y, Seshimo F, Higuchi T, Yamazaki H, Hasegawa C, et al. (2005)
Development of a simple method for predicting the levels of di(2-ethylhexyl) phthalate migrated from PVC medical devices into pharmaceutical solutions.
Int J Pharm 2005; 298:126-42.
9 Hanawa T, Muramatsu E, Asakawa K, Suzuki M, Tanaka M, et al. (2000)
Investigation of the release behavior of diethylhexyl phthalate from the polyvinyl-chloride tubing for intravenous administration.
Int J Pharm; 210:109-15.
10 Hanawa T, Endoh N, Kazuno F, Suzuki M, Kobayashi D, et al. (2003)
Investigation of the release behavior of diethylhexyl phthalate from polyvinyl chloride tubing for intravenous administration based on HCO60.
Int J Pharm; 267:141-9.
11 Loff S, Kabs F, Witt K, Sartoris J, Mandl B, Niessen KH, Waag KL (2000)
Polyvinylchloride infusion lines expose infants to large amounts of toxic plasticizers.
J Pediatr Surg; 35:1775-81.
12 Loff S, Kabs F, Subotic U, Schaible T, Reinecke F, Langbein M (2002)
Kinetics of diethylhexylphthalate extraction from polyvinylchloride-infusion lines.
JPEN J Parenter Enteral Nutr; 26:305-9.
13 Loff S, Subotic U, Reinicke F, Wischmann H, Brade J (2004)
Extraction of Di-ethylhexyl-phthalate from Perfusion Lines of Various Material, Length and Brand by Lipid Emulsions.
J Pediatr Gastroenteral Nutr; 39:341-345.
14 Bourdeaux D, Sautou-Miranda V, Bagel-Boithias S, Boyer A, Chopineau J (2004)
Analysis by liquid chromatography and infrared spectrometry of di(2-ethylhexyl)phthalate released by multilayer infusion tubing.
J Pharm Biomed Anal; 35:57-64.
15 de Lemos ML, Hamata L, Vu T. (2005)
Leaching of diethylhexyl phthalate from polyvinyl chloride materials into etoposide intravenous solutions.
J Oncol Pharm Pract;11(4):155-7
16 Trissel LA, Pearson SD (2/1994)
Storage of lorazepam in three injectable solutions in polyvinyl chloride and polyolefin bags.
Am J Hosp Pharm; 1;51(3):368-72.
17 FDA Public Health Notification: PVC Devices Containing the Plasticizer DEHP.
18 Rubin RJ, Schiffer CA (1976)
Fate in humans of the plasticizer, di-2-ethylhexyl phthalate, arising from transfusion of platelets stored in vinyl plastic bags.
Transfusion; 16(4): 330–335.
19 Jaeger RJ, Rubin RJ (1972)
Migration of a phthalate ester plasticizer from polyvinyl chloride blood bags into stored human blood and its localization in human tissues.
N Engl J Med; 287(22): 1114–1118.
20 Sjöberg P, Bondesson U, Sedin G and Gustafsson J (1985)
Disposition of di- and mono- 2ethylhexyl)phthalate in newborn infants subjected to exchange transfusions.
Eu J Clin. Invest; 15: 430-436.
21 Easterling RE, Johnson E, Napier EA (1974)
Plasma extraction of plasticizers from “medical grade” polyvinylchloride tubing.
Proc Soc Exp Biol Med 147: 572–574.
22 Bagel S, Dessaigne B, Bourdeaux D, Boyer A, Bouteloup C, Bazin JE, Chopineau J, Sautou V. (2011)
Influence of lipid type on bis (2-ethylhexyl)phthalate (DEHP) leaching from infusion line sets in parenteral nutrition.
JPEN J Parenter Enteral Nutr; 35(6): 770-5
23 Health Canada (2002) An exposure and toxicity assessment. Medical Devices Bureau, Therapeutic Products Directorate, Health Products and Food Branch, Ottawa, Canada.
24 Pearson SD, Trissel LA (1993)
Leaching of diethylhexyl phthalate from polyvinyl chloride containers by selected drugs and formulation components.
Am J Hosp Pharm; 50:1405-9.
25 Lee MG, Fenton-May V (1981)
Absorption of isosorbide dinitrate by PVC infusion bags and aministration sets.
J Clin Hosp Pharm; Sep;6 (3):209-11.
26 Beitz C, Bertsch T, Hannak D, Schrammel W, Einberger C, Wehling M (8/2005)
Compatibility of plastics with cytotoxic drug solutions—comparison of polyethylene with other container materials.
Int Journ of Pharm; (1)185: 113–121.
27 Treleano A, Wolz G, Brandsch R, Welle F (3/2009)
Investigation into the sorption of nitroglycerin and diazepam into PVC tubes and alternative tube materials during application.
Int J Pharm; 18; 369(1-2):30-7.
28 Martens HJ, De Goede PN, Van Loenen AC (2/1990)
Sorption of various drugs in polyvinyl chloride, glass, and polyethylene-lined infusion containers.
Am J Hosp Pharm; 1990 Feb;47(2):369-73.
29 Frenette AJ, MacLean RD, Williamson D, Marsolais P, Donnelly RF (9/2011)
Stability of levothyroxine injection in glass, polyvinyl chloride, and polyolefin containers.
Am J Health Syst Pharm; 15;68(18):1723-8.
30 Hedley AJ, Wong TW, Hui LL, Malisch R, Nelson EA (2/2006)
Breast milk dioxins in Hong Kong and Pearl River Delta.
Environ Health Perspect; 114(2):202-8.
31 WHO Factsheet no 225, 2010,
Dioxins and their effect on human health, May 2012
32 http://www.pvc.org/en/p/Health_concerns_about_Phthalate_plasticisers
33 Zhang LD, Li HC, Chong T, Gao M, Yin J, Fu DL, Deng Q, Wang ZM. (2014)
Prepubertal exposure to genistein alleviates di-(2-ethylhexyl) phthalate induced testicular oxidative stress in adult rats.
Biomed Res Int; 2014: 598630. doi: 10.1155/2014/598630.
34 Kay VR, Bloom MS, Foster WG. (2014)
Reproductive and developmental effects of phthalate diesters in males.
Crit Rev Toxicol; 44(6): 467-98.
35 Pflieger-Bruss S, Schuppe HC, Schill WB. (2004)
The male reproductive system and its susceptibility to endocrine disrupting chemicals.
Andrologia; 36(6): 337-45.
36 Mallow EB, Fox MA. (2014)
Phthalates and critically ill neonates: device-related exposures and non-endocrine toxic risks.
J Perinatol; 34(12): 892-7.
37 Pak VM, Nailon RE, McCauley LA. (2007)
Controversy: neonatal exposure to plasticizers in the NICU.
MCN Am J Matern Child Nurs; 32(4): 244-9.
38 Marie C, Vendittelli F, Sauvant-Rochat MP. (2015)
Obstetrical outcomes and biomarkers to assess exposure to phthalates: A review.
Environ Int; 83: 116-36.
39 Rusyn I, Corton JC. (2012)
Mechanistic considerations for human relevance of cancer hazard of di(2-ethylhexyl) phthalate.
Mutat Res; 750(2): 141-58
40 Tickner JA, Schettler T, Guidotti T, McCally M, Rossi M. (2001)
Health risks posed by use of Di-2-ethylhexyl phthalate (DEHP) in PVC medical devices: a critical review.
Am J Ind Med; 39(1): 100-11.
41 National toxicology programm, the US department of health and human services (11/2006) Center for the evaluation of risks to human reproduction:
NTP-CERHR Monograph on the Potential Human Reproductive and Developmental Effects of Di(2-Ethylhexyl) Phthalate (DEHP).
NIH Publication No. 06 – 4476.
42 Fachinformation Taxol (1/2009), Abschnitt 6.2. Brystol-Meyers-Squibb.
43 Panknin HT.
Particle release from infusion equipment: etiology of acute venous thromboses.
Kinderkrankenschwester. 2007;26:407-8.
44 Danschutter D, Braet F, Van Gyseghem E, Hachimi-Idrissi S, Van Bruwaene B, Moloney-Harmon P, Huyghens L.
Di-(2-ethylhexyl) phthalate and deep venous thrombosis in children: a clinical and experimental analysis.
Pediatrics. 2007;119:e742-53.
45 IARC (1997)
Polychlorinated dibenzo-p-dioxins and polychlorinated dibenzofurans.
IARC Monogr Eval Carcinog Risks Hum 69:1–343.
46 Steenland K, Bertazzi P, Baccarelli A, Kogevinas M (2004)
Dioxin revisited: developments since the 1997 IARC classification of dioxin as a human carcinogen.
Environ Health Perspect 112:1265–1268.
47 IARC Working Group on the Evaluation of Carcinogenic Risks to Humans:
Polychlorinated Dibenzo-Para-Dioxins and Polychlorinated Dibenzofurans.
IARC Monogr Eval Carcinog Risks Hum. 1997;69:1-631.
48 EPA 2012
Reanalysis of key issues related to dioxin toxicity and response to NAS comments
49 Bernard L, Décaudin B, Lecoeur M, Richard D, Bourdeaux D, Cueff R, Sautou V; Armed Study Group. (2014)
Analytical methods for the determination of DEHP plasticizer alternatives present in medical devices: a review.
Talanta; 129: 39-54
50 Fischer CJ, Bickle Graz M, Muehlethaler V, Palmero D, Tolsa JF. (2013)
Phthalates in the NICU: is it safe?
J Paediatr Child Health;49(9):E413-9
51 European Commission, T. S. C. o. M. P. a. M. D. (2002).
“Opinion on Medical Devices Containing DEHP Plasticised PVC; Neonates and Other Groups Possibly at Risk from DEHP Toxicity.”
52 Greenpeace International (2003) PVC-Free Future:
A Review of Restrictions and PVC-free Policies Worldwide.
53 Änderung im Anhang der REACH-Regulation (PDF), Stand 17. Februar 2011
54 REACH - Registration, Evaluation, Authorisation of Chemicals (2007)
55 RICHTLINIE 2007/47/EG DES EUROPÄISCHEN PARLAMENTS UND DES RATES
vom 5. September 2007 zur Änderung der Richtlinien 90/385/EWG des Rates zur Angleichung der Rechtsvorschriften der Mitgliedstaaten über aktive implantierbare medizinische Geräte und 93/42/EWG des Rates über Medizinprodukte sowie der Richtlinie 98/8/EG über das Inverkehrbringen von Biozid-Produkten
56 Emerson C, ALP Australia Bans Phthalates in Toys.
57 PVC: The Poison Plastic. PVC Governmental Policies around the World.
58 Referenz-Nr.: 9211/0506 DEHP als Weichmacher in Medizinprodukten aus PVC.
Erstellt: 22.05.2006
59 Health Canada. Consumer Product Safety. (2007) Proposal for legislative action on di(2-ethylhexyl) phthalate under the Hazardous Products Act.
60 http://chm.pops.int
61 Japanese Makers to Switch from PVC to Eco-Based Containers’, Nikkei, Tokyo, January 14, 1998.
62 FoodBev.com, 31.01.2012
63 http://www.plasticsnews.com/headlines2.html?ncat=&id=24284
64 Health Care Without Harm (2003)
Glanzing Clinic in Vienna is First PVC-Free Pediatric Unit Worldwide.
Press release (June 13, 2003).
65 Initiative „Schadstofffreies Krankenhaus“ gegen PVC-haltige Medizinprodukte.
Deutsches Ärzteblatt, Ausgabe 15. November 2006;
66 OSPAR List of Chemicals for Priority Action (Revised 2011),
Reference number 2004-12;
67 Wirnitzer, U (2011)
Non-Clinical Testing of the Plasticizer Di-2-ethylhexyl-terephtalate (DEHT) under Clinically relevant Conditions.
ITO Symposium 15.-16. Sep 2011.
68 Wirnitzer U, Rickenbacher U, Katerkamp A, Schachtrupp A.
Systemic toxicity of di-2-ethylhexyl terephthalate (DEHT) in rodents following four weeks of intravenous exposure.
Toxicol Lett. 2011 Aug 10;205(1):8-14.
69 Unpublished data, Eastman Chemical Company.
70 https://www.accessdata.fda.gov/scripts/fdcc/?set=ENV-FCN
71 Stoffers, N.H., Stoermer, A., Bradley, E.L., Brandsch, R., Cooper, I., Linssen, J.P.H., Franz, R., 2004.
Feasibility study for the development of certified reference materials for specific migration testing: Part 1. Initial migration concentration and specific migration.
Food Addit. Contam. 21, 1203–1216.
72 Stoffers, N.H., Brandsch, R., Bradley, E.L., Cooper, I., Dekker, M., Stoermer, A., Franz, R., 2005.
Feasibility study for the development of certified reference materials for specific migration testing: Part 2. Estimation of diffusion parameters and comparison of experimental and predicted data.
Food Addit. Contam. 22, 173–184.
73 European Pharmacopoeia monograph 3.1.4 of the Polyethylene without additives for containers for preparations for parenteral use and for ophthalmic preparations.
74 Kaiser J., Krämer I.
Physicochemical stability of diluted trastuzumabinfusion solutions in polypropylene infusion bags.
Int J Pharm Compounding 2011 15:6 (515-520).
75 Menard C., Bourguignon C., Schlatter J., Vermerie N., Schlatter J.
Stability of Cyclophosphamide and Mesna Admixtures in Polyethylene Infusion Bags.
Annals of Pharmacotherapy 2003 37:12 (1789-1792).
76 Arsène M., Favetta P., Favier B., Bureau J., Favetta P.
Comparison of ceftazidime degradation in glass bottles and plastic bags under various conditions.
Journal of Clinical Pharmacy and Therapeutics 2002 27:3 (205-209).
77 Jenke D, Couch T, Gillum A, Sadain S.
Modeling of the solutioninteraction properties of plastic materials used in pharmaceutical product container systems.
PDA J Pharm Sci Technol. 2009 Jul-Aug;63(4):294-306.
78 Römpp Lexikon Chemie, 9. Auflage 1992
79 The Straits Times, Thu, Oct 29, 2009
80 The costs of myocardial infarction-a longitudinal analysis using data from a large German health insurance company Reinhold T, Lindig C, N. Willich S, Brüggenjürgen B. Journal of Public Health 2011 19:6 (579-586)
81 Nephrol Dial Transplant (2009) 24: 3209–3215. The Pan-Thames EPS study: treatment and outcomes of encapsulating peritoneal sclerosis. Gowrie Balasubramaniam, Edwina A. Brown, Andrew Davenport, Hugh Cairns, Barbara Cooper, Stanley L. S. Fan, Ken Farrington, Hugh Gallagher, Patrick Harnett, Sally Krausze and Simon Steddon.
82 Prevalence rates and costs of metabolic syndrome and associated risk factors using employees' integrated laboratory data and health care claims. Birnbaum H.G., Mattson M.E., Kashima S., Williamson T.E. Journal of Occupational and Environmental Medicine 2011 53:1 (27-33)
83 Health economics perspective of the components of the cardiometabolic syndrome Tamariz L., Palacio A., Florez H., Tamariz L., Palacio A., Yang Y., Parris D., Florez H., Tamariz L., Palacio A., Florez H., Ben-Joseph R.
84 Economic Analysis of Infant vs Postpubertal Orchiopexy to Prevent Testicular Cancer. Hsieh M.H., Roth D.R., Meng M.V. Urology 2009 73:4 (776-781)
85 Staged reconstruction of hypospadias with chordee: Outcome and costs. Svensson H, Reychman M, Åberg M, Troëng T, Svensson H. Scandinavian Journal of Plastic and Reconstructive Surgery and Hand Surgery 1997 31:1 (51-55)
86 One-year costs in patients with a history of or at risk for atherothrombosis in the United States. Mahoney E.M., Wang K., Cohen D.J., Hirsch A.T., Alberts M.J., Eagle K., Mosse F., Jackson J.D., Steg P.G., Bhatt D.L., REACH Registry Investigators Circulation. Cardiovascular quality and outcomes 2008 1:1 (38-45)













