Mikrobiológiai szennyeződés
A mikrobiológiai fertőzés az olyan anyagoknak, mint például baktériumok, élesztőgombák, férgek, vírusok, prion, protozoonok vagy ezek méreganyagainak nem várt szervezetbe jutását jelenti.1,2
„A nozokomiális fertőzéseket” — másnéven „kórházban szerzett ártalmakat” a következőképpen definiálhatjuk:
A fertőzés megjelenése olyan betegben, akiben a kórokozó a kórházba, illetve egyéb egészségügyi ellátó intézménybe kerülésekor nem volt jelen. Ide soroljuk azokat a fertőzéseket is, amikor a tünetek csak a kórházból való elbocsátás után jelentkeznek és a foglalkozási bántalmakat is, melyeket az egészségügyi szakszemélyzet szenved el3
A kórokozók egyes típusai
A Katéterek Által Okozott Infekció (CR-BSI) definíciója
Az MRSA előfordulása és gyakorisága
A multirezisztencia fogalma
Tudta?

(1) Pittet, Didier; „Adapt to adopt; TEDxPlaceDesNations“, under https://www.youtube.com/watch?v=5tgH0uTqqcE (accessed at 2 May 2016)
(2) WHO; Presentation: WHO_Facts_DRT661; „Health-Care Associated Infection and Hand Hygiene Improvement - Slides for the Hand Hygiene Co-ordinator of the WHO“ http://www.who.int/gpsc/country_work/gpsc_ccisc_fact_sheet_en.pdf
Okai
Szennyeződés akkor keletkezhet, amikor a kórokozók előre nem várt módon kerülnek a szervezetbe egy, a testen lévő nyílás által, ahol aztán elkezdenek nőni és káros hatásukat kifejteni. Számos lehetőség van a szervezetbe jutásra.
Potenciális források, bejutási utak és átviteli módok
Infúzióval kapcsolatos fertőzések
Egészségügyi következmények
A nozokomiális infekciók világszerte problémát jelentenek és egyformán érintik a fejlett és a fejlődő országok lakóit. Az egészségügyi ellátás kapcsán szerzett fertőzések kétségtelenül megnövelik a megbetegedések számát és a halálozási arány is nő. Az infekció fokozott megterhelést jelent az egyes betegeknek épp úgy, ahogyan a népegészségügynek. Egy WHO támogatásával készült – a fertőzések gyakoriságát vizsgáló - tanulmány, amelyet 14 ország 55 kórházában végeztek és a 4 nagy régiót foglalja magába (Európa, a Földközi-tenger keleti része, Dél-kelet Ázsia és a Csendes-óceán nyugati térsége) 8,7 %-os gyakoriságát mutatta a nozokomiális infekciók előfordulásának. Bármely időintervallumot tekintünk, átlagosan 1,4 millió ember szenved világszerte a kórházban szerzett fertőzések komplikációitól.15
A legmagasabb számú megbetegedésről a Földközi-tenger keleti részén és Dél-Kelet Ázsia területein számoltak be (11,8 és 10,0 %) , illetve 7,7 és 9,0 % -os gyakorisággal az európai és a Csendes-óceán nyugati térségeiben.16
A leggyakoribb kórházban szerzett infekciók közé a sebészeti beavatkozások után fellépő fertőzéseket, a vizeletkiválasztó szervrendszert és az alsó légutakat érő fertőzéseket soroljuk.
A WHO tanulmánya és egyéb felmérések is igazolják, hogy a nozokomiális infekciók előfordulása intenzív osztályokon, sebészeti részlegeken és ortopédiai osztályokon a legmagasabb.Az idős, kemoterápiára szoruló vagy alapbetegséggel rendelkező betegek különösen veszélyeztetettek.3
A szennyeződés és az ebből következő fertőzés megjelenhet lokálisan vagy szisztémásan.
- Helyi fertőzések esetében sebek infekcióját, bőrirritációt és a szúrcsatorna gyulladását láthatjuk.
- Ha a kórokozók bejutnak a szisztémás keringésbe, septicaemia, sepsis és septikus shock lehet a következmény. Ily módon a kórokozók eljuthatnak a szervekhez, végtagokhoz, elégtelenséget okozva azok működésében, okozhat endocarditist, osteomyelitist, utóbbi amputációhoz is vezethet.17,18
Ezeket az állapotokat minden esetben kezelni kell, további vizsgálatokat kell végezni, amelyek a beteg számára pszichés megterheléssel, stresszel, mellékhatásokkal, fájdalommal járhatnak. Sajnálatos módon néhány esetben maradandó károsodással kell számolnunk, mely az életminőség romlását okozza.
Mindezekkel együtt szükségessé válhat a kórházi tartózkodás meghosszabbítása. Egy felmérés19 szerint az átlagos kórházi tartózkodás ideje sebészeti fertőzések esetében 8,2 nappal hosszabbodott, a következő eloszlással: 3 nap a nőgyógyászati műtéten átesettek esetében, 9,9 nap az általános sebészeten, ortopédiai műtétek esetében pedig a legmagasabb, 19,8 nap.
A 2007. május 8-án elvégzett EPIC II pontprevalencia-vizsgálat a kritikus állapotban lévő betegek esetében érdekes eredménnyel szolgált. Staphylococcus aureus által fertőzött betegek túlélését vizsgálták, a methicillin-rezisztencia szerepét figyelmbe véve. A felmérés napján 7,087 (51 %) volt fertőzöttnek tekinthető a vizsgált 13, 796 betegből. 494-en szenvedtek MRSA fertőzéstől, 505-en MSSA fertőzéstől. Az intenzív osztály halálozási mutatója 29,1 % és 20,5 % volt a két esetre vetítve (P<0.01), miközben a standard kórházi mutató 36.4 % és 27.0 % (P<0.01) volt. Az MRSA-val kapcsolatos kórházi mortalitás vizsgálata közben megnövekedett számadatokat találtak 1.46 (95 % CI 1.03-2.06) (P=0.03).
Az intenzív osztályon fekvő betegek esetében 50%-kal nagyobb a mortalitás esélye MRSA miatt, mint MSSA fertőzés következtében.20 Más eredmények alapján a véráramot érintő fertőzések halálozási aránya 10-25 % között van, míg a septicus sokk esetében ez 40-60 %.21 Ezek alapján kijelenthetjük, hogy a nozokomiális infekciók a leggyakrabban előforduló halálokok között szerepelnek.22
Gazdasági következmények
Az orvosi eszközök és infúziós oldatok szennyeződésének megelőzése, és ezzel a súlyos fertőzések, valamint a szepszis elkerülése kiemelt fontossággal bír a kórházakban, és jelentős megtakarításokat eredményezhet az egészségügyi szolgáltató számára.
A nozokomiális infekciók hatásai
Még a nem halálos kimenetelű fertőzések is a terápiás és diagnosztikus eszköztár nagyobb igénybevételét jelentik, például laboratóriumi munka, hemokultura, röntgenvizsgálat, antibiotikumok és katecholamin-támogatás tekintetében. Mindehhez hozzájárul a már előzőekben taglalt hosszabb kórházi tartózkodás és megnövekedett költségek.48,49,50
A potenciális kockázatokkal kapcsolatos költségek
A költségek az intenzív osztályokon nagy százalékban állandóak, változást leginkább az intenzív osztályon folyó kezelés időtartama eredményezhet. Az átlag napi költség egy beteg esetében, fejlett technológiával rendelkező országban 1200 euró, amelyet 1989 és 2001 között végzett tanulmányok igazolnak, 2003-as árfolyamon számolva).
A betegek hosszabb intenzív osztályos tartózkodást igényelnek, és az ellátás költsége kétségtelennül nagyobb abban az esetben, mikor fertőzéssel állunk szemben. Az Egyesült Államokban a sepsis terápiájának direkt költségeit vizsgáló tanulmányok szerint a költségbecslések 34,000 euróra rúgtak, míg európai tanulmányok szerint ezek a költségek alacsonyabbak: 23,000-29,000 €. Ezek a közvetlen költségek azonban még így is 20-30%-át teszik ki a teljes összegnek, a maradék 70-80 %-ot az elhalálozás miatti termelés, termelékenység csökkenése adja.51
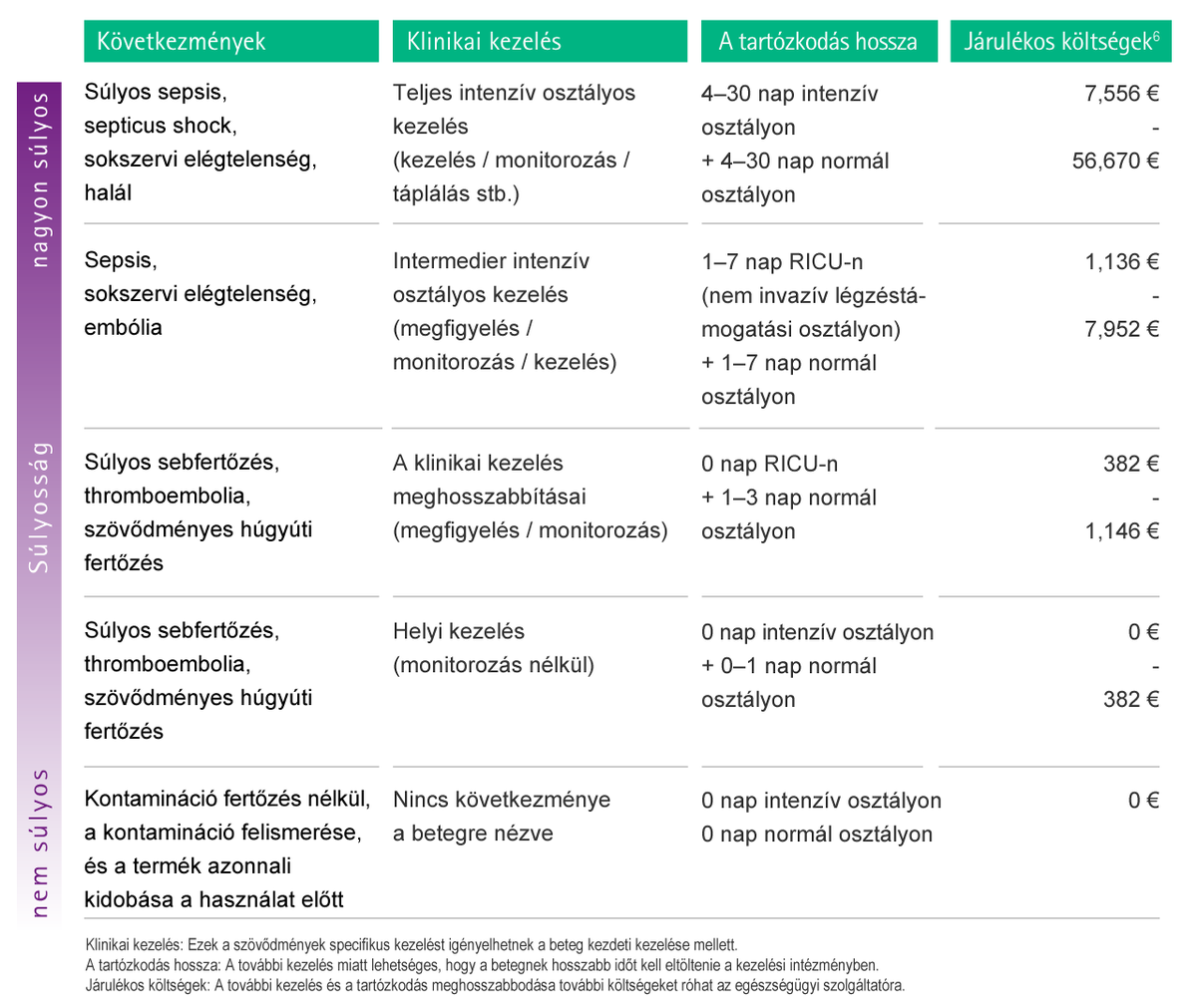
4. ábra: A légembólia által okozott szövődmények miatt fellépő lehetséges járulékos költségek becslése. Az egyes szövődmények költségszámításhoz történő besorolásának megkönnyítése érdekében súlyossági fokozatokat vezettünk be. RICU Nem invazív légzéstámogatási osztály (Respiratory Intermediate Care Unit)
Az alábbi ábra a kórházi fertőzésekkel kapcsolatos költségeket mutatja be vázlatos formában.52
Megelőzés
A szennyeződések és fertőzések megelőzése az elmúlt években a figyelem középpontjába került. A nozokomiális infekciók igen súlyos következményei és a gazdasági hatások együttesen hozzájárulnak ahhoz, hogy új irányelvek kerüljenek kidolgozásra, amelyek segítségével a jövőben csökkenthető lesz ezen megbetegedések száma.3,6,9,10,23,24,25
Oktatás és gyakorlás
Monitorizálás - megfigyelés
Kezelési szempontok
Műszaki és technikai megoldások
Kiemelt biztonsági termékek
Tudományos bizonyíték
1 Ghiglione JF, Martin-Laurent F, Pesce S. (2015) Microbial ecotoxicology: an emerging discipline facing contemporary environmental threats. Environ Sci Pollut Res; DOI 10.1007/s11356-015-5763-1
2 Gabriel J. (2008) Infusion therapy. Part two: Prevention and management of complications. Nurs Stand; 22(32): 41-8
3 World Health Organization 2002
4 Ducel G. Les nouveaux risques infectieux. Futuribles. 1995;203:5–32
5 Guembe M, Martín-Rabadán P, Echenagusia A, Camúñez F, Rodríguez-Rosales G, Simó G, Echenagusia M, Bouza E. (2012) How should long-term tunneled central venous catheters be managed in microbiology laboratories in order to provide an accurate diagnosis of colonization? J Clin Microbiol;50(3):1003-7
6 O‘Grady NP, Alexander M, Dellinger EP, Gerberding JL, Heard SO, Maki DG, Masur H, McCormick RD, Mermel LA, Pearson ML, Raad II, Randolph A, Weinstein RA. 2002
7 European Centre for Disease Prevention and Control. Prevalence of MRSA in Europe 2008
8 Hidron AI, Edwards JR, Patel J, Horan TC, Sievert DM, Pollock DA, Fridkin SK; National Healthcare Safety Network Team; Participating National Healthcare Safety Network Facilities. (2008) NHSN annual update: antimicrobial-resistant pathogens associated with healthcare-associated infections: annual summary of data reported to the National Healthcare Safety Network at the Centers for Disease Control and Prevention, 2006-2007. Infect Control Hosp Epidemiol. 2008 Nov;29(11):996-1011
9 Centers for Disease Control and Prevention (CDC)
10 Hebert C, Weber SG. (2011) Common approaches to the control of multidrug-resistant organisms other than methicillin-resistant Staphylococcus aureus (MRSA). Infect Dis Clin North Am. 2011 Mar;25(1):181-200
11 Shah H, Bosch W, Thompson KM, Hellinger WC. (2013) Intravascular catheter-related bloodstream infection. Neurohospitalist; 3(3): 144-51
12 Mermel LA. (2011) What is the predominant source of intravascular catheter infections? Clin Infect Dis. 2011 Jan 15;52(2):211-2
13 Rosado V, Romanelli RM, Camargos PA. (2011) Risk factors and preventive measures for catheter-related bloodstream infections. J Pediatr (Rio J); 87(6): 469-77
14 Jamieson EM, McCall JM, Whyte LA. Practice 21: Intravenous therapy. In: Jamieson EM, McCall JM, Whyte LA. Clinical nursing practices. 5. Edition, Edinburgh [u.a.]: Elsevier Churchill Livingstone 2007; 169-176
15 WHO, 2002, Prevention of hospital-acquired infections. A practical guide. 2nd edition.
16 Khan, Hassan Ahmed; Baig, Fatima Kanwal; Mehboob, Riffat (2017): Nosocomial infections. Epidemiology, prevention, control and surveillance. In Asian Pacific Journal of Tropical Biomedicine 7 (5), pp. 478–482. DOI: 10.1016/j.apjtb.2017.01.01916
17 Uslusoy E., Mete S. (2008) Predisposing factors to phlebitis in patients with peripheral intravenous catheters: a descriptive study. J Am Acad Nurse Pract; 20(4): 172-80
18 Bouchoucha S, Benghachame F, Trifa M, Saied W, Douira W, Nessib MN, Ghachem MB. (2010) Deep venous thrombosis associated with acute hematogenous osteomyelitis in children. Orthop Traumatol Surg Res; 96(8): 890-3
19 Raad I. (1998) Intravascular-catheter-related infections.Lancet; 351(9106): 893-8.
20 Hanberger H, Walther S, Leone M, Barie PS, Rello J, Lipman J, Marshall JC, Anzueto A, Sakr Y, Pickkers P, Felleiter P, Engoren M, Vincent JL; EPIC II Group of Investigators. (2011) Increased mortality associated with methicillin-resistant Staphylococcus aureus (MRSA) infection in the intensive care unit: results from the EPIC II study. Int J Antimicrob Agents; 38(4): 331-5
21 Rosenthal VD, Maki DG. (2004) Prospective study of the impact of open and closed infusion systems on rates of central venous catheter-associated bacteremia. Am J Infect Control; 32(3): 135-41.
22 Gastmeier P, Geffers C, Brandt C, Zuschneid I, Sohr D, Schwab F, Behnke M, Daschner F, Rüden H. (2006) Effectiveness of a nationwide nosocomial infection surveillance system for reducing nosocomial infections. J Hosp Infect; 64(1): 16-22
23 Zingg W, Holmes A, Dettenkofer M, Goetting T, Secci F, Clack L, Allegranzi B, Magiorakos AP, Pittet D; systematic review and evidence-based guidance on organization of hospital infection control programmes (SIGHT) study group. (2015) Hospital organisation, management, and structure for prevention of health-care-associated infection: a systematic review and expert consensus. Lancet Infect Dis. 2015; 15(2): 212-24
24 Sax H, Clack L, Touveneau S, Jantarada Fda L, Pittet D, Zingg W; PROHIBIT study group. (2013) Implementation of infection control best practice in intensive care units throughout Europe: a mixed-method evaluation study. Implement Sci; 8: 24
25 World Health Organization. 2004
26 Royal College of Nursing (RCN). 2010
27 World Health Organization. 2009 World Health Organization. WHO Guidelines on Hand Hygiene in Health Care. WHO Library Cataloguing-in-Publication Data,
28 MMWR Morbitity and Mortality Weekly Report. 2002 Morbitity and Mortality Weekly Report. Guideline for Hand Hygiene in Health-Care Settings. Recommendations of the Healthcare Infection Control Practices Advisory Committee and the HICPAC/SHEA/APIC/IDSA Hand Hygiene Task Force. Recommendations and Reports, Oct 25, 2002, (51) No. RR-16
29 Grayson ML, Jarvie LJ, Martin R, Johnson PD, Jodoin ME, McMullan C, Gregory RH, Bellis K, Cunnington K, Wilson FL, Quin D, Kelly AM, 2008
33 Royal College of Nursing. 2005
34 Scales K. Vascular access: a guide to peripheral venous cannulation. Nurs Stand. 2005; 19(49): 48-52
35 NIOSH. Preventing Occupational Exposures to Antineoplastic and other Hazardous Drugs in Healthcare Settings. 2004
bloodstream infection. International Journal of Antimicrobial Agents 2008; 31: 161-165
52 Plowman RP, Graves N, Robers JA. Hospital Aquired Infection. Office of Health Economics, London 1997
16











