Részecskeszennyeződés
A részecskeszennyeződés idegen, mozgékony és nem oldódó részecskék önkéntelen (váratlan) jelenlétét jelenti egy parenterális oldatban.1,2 Ezen részecskék különböző méretűek lehetnek: szabad szemmel érzékelhetőek (rendszerint ≥ 50 μm) vagy alig láthatóak. Általánosságban 2-50 μm nagyságúak. A láthatatlan részecskék kimutatásához különleges vizsgálatokra van szükség.
Tudta?

(1) Ortolani GA, Russell RL, Angelbeck JA, Schaffer J, Wenz B. (2004) Contamination control in nursing with filtration. Part 1: filters applied to intravenous fluids and point-of-use hospital water. J Infus Nurs; 27(2): 89-103
(2) Anonymus [No authors listed]. (2004) Risks due to particles in infusion therapy--experts promote use of infusion filters. Krankenpfl J. 2004; 42(3-4): 97
(3) Lehr HA, Brunner J, Rangoonwala R, Kirkpatrick CJ. (2002) Particulate matter contamination of intravenous antibiotics aggravates loss of functional capillary density in postischemic striated muscle. Am J Respir Crit Care Med; 165:514-520
Okai
Az infúziós oldatok részecskeszennyeződésének számos oka ismert. Ez annak köszönhető, hogy a gyógyszerek különböző kiszerelésben kaphatók (például fiolák, ampullák, előre töltött zsákok és előre kevert oldatok), használatuk pedig igen sokrétű.
Ennek következményeként sokféle részecskeszennyeződés jelenhet meg:
Üveg
Amennyiben az üvegampulla tartalmát tűvel (például 18 G) távolítjuk el, apró üvegrészecskék juthatnak át a tűn keresztül a fecskendőbe, onnan pedig a betegbe. Ez a kockázat akkor is fennáll, ha a gyógyszert rutinszerűen injekció portos vénás kanülön keresztül juttatjuk a betegbe. Ez a módszer egy közismert biztonsági intézkedés, amely a kórházi személyzet körében előforduló tűszúrásos balesetek csökkentésére szolgál.3,4
Műanyag
Műanyag szennyeződés is gyakran előfordul mely származhat:
- az infúziós zsák alapanyagából
- az injekciós nyílás szintjéről (éles eszközökkel való használat eredményeképpen)
Gumi
A tű átszúrása a gyógyszeres ampulla dugaszán vagy az infúziós zsákon levághatja a dugasz egy darabkáját. Ez a darabka a gyógyszerbe vagy az infúziós oldatba kerülhet. Ha a részecske pici vagy rejtve marad (pl. a címke mögött, a színes ampulla vagy a hasonló színű háttér miatt), a szennyeződés észrevétlen maradhat. Így a részecskét felszívhatjuk a fecskendőbe és azon keresztül a betegbe juthat.5
Feloldatlan részecskék/gyógyszerek
A gyógyszerek vagy az infúziós oldatok feloldatlan szilárd összetevői is eredményezhetnek részecske szennyeződést.6,7
Egészségügyi következmények
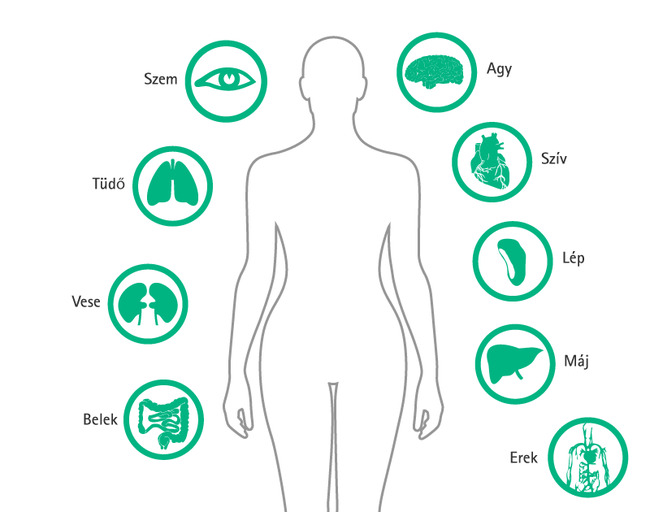
1. ábra: Az intravénás folyadékok szemcsés szennyeződése által leginkább érintett részek és szervek az emberi szervezetben.
Minden olyan részecske az intraluminális térben, amit nem fog fel egy szűrő, behatol az emberi testbe. Ezek a műanyag, üveg- vagy gumirészecskék kedvezőtlen hatást idézhetnek elő, különösen krónikus betegeknél.
Az 1.5 μm méretű részecskék elzáródást okozhatnak a betegeknél, míg a 6 μm méretűek akár az egészséges embereknél is.7,8,11
Általában véve a különböző szervek károsodásáról számolnak be, mint például a tüdő, vesék, máj és lép1,6 de szembetűnő a súlyos betegek kiemelt érintettsége.8-11 Az előzetesen szervi károsodást elszenvedett betegek különösen érzékenyek, mivel a részecskék ronthatnak a már csökkent mikrokeringésen.8,11
Egy másik klinikai tünet, amelyet az üvegampullákból bekerült üvegrészecskék okozhatnak, az a vénagyulladás (phlebitis).7,8,12 Phlebitis esetén meleg, fájdalmas, dagadt és bőrpírrel járó tüneteket észlelünk a bejutás helyén.13
Gazdasági következmények
Tekintettel a jelentős számú szövődményekre, kijelenhető, hogy a betegek részecskeszennyeződése (műanyag, üveg, gumi) megnövelheti a kórházi tartózkodás hosszát, illetőleg a költségeket is.
A potenciális kockázatokkal kapcsolatos költségek
A klinikai ellátás költségei, valamint a kórházi tartózkodás időtartama alapján megbecsülhető a egészségügyi intézmények kockázatokkal kapcsolatos költségei. Az átlagos napi ellátási költségek alapján könnyen kiszámolhatóak a várható költségek.
Az alábbi 2. ábra az egyes ilyen jellegű szövődményekkel kapcsolatos számítások eredményét mutatja be.
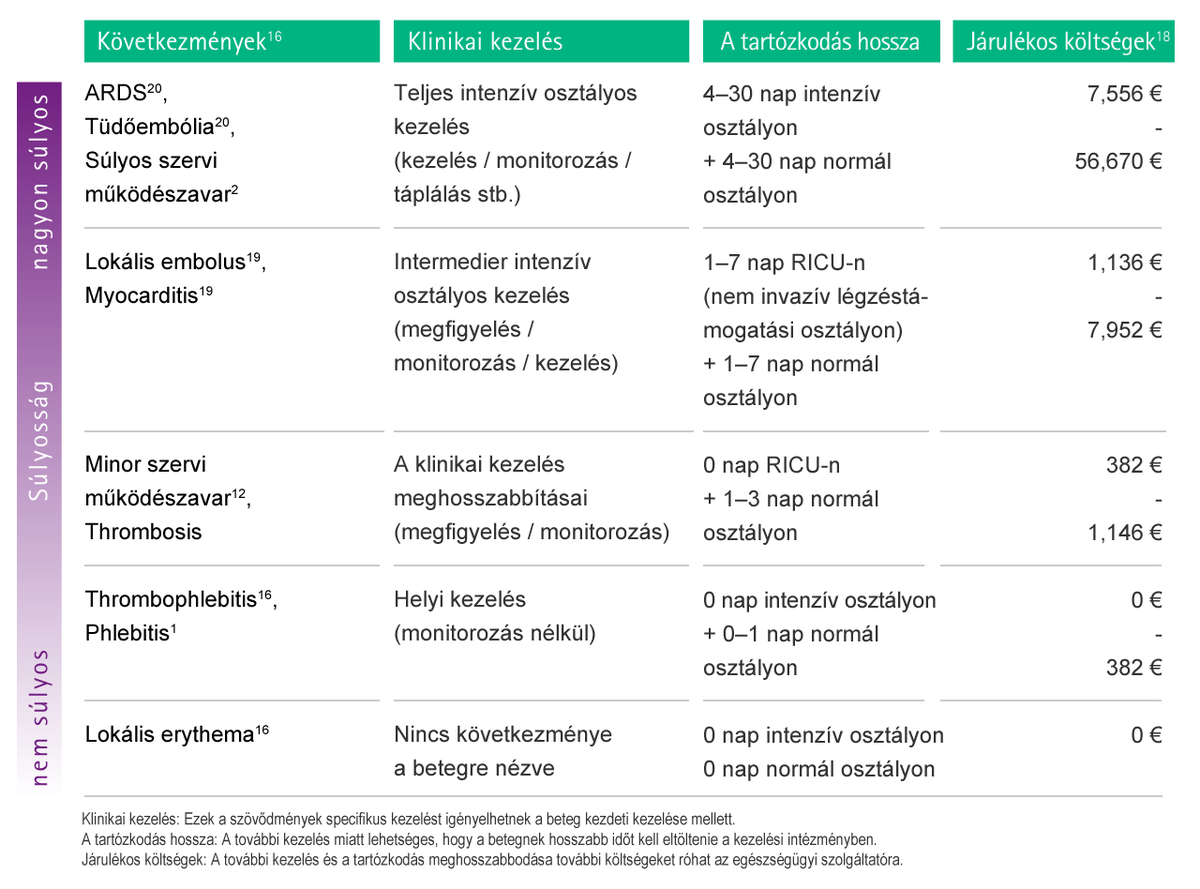
2. ábra: A szemcsés szennyeződés által okozott szövődményekből eredő becsült potenciális többletköltségek. A költségszámítás során az egyes szövődményeket az adott szövődmény súlyossági szintjének megfelelően vettük figyelembe. ARDS: Akut respirációs distressz szindróma. RICU: Köztes respirációs betegellátó osztály
A közvetlen és közvetett szövődmények súlyosságától függően a beteg légúti rendszerébe került idegen szemcsés szennyeződések esetenként akár 56.670 EUR többletköltséggel járhatnak az egészségügyi szolgáltató számára.16-19
Megelőzés
A részecskeszennyeződés megelőzésének érdekében számos lehetőség közül választhatunk, mint pl.:
- minőségi termékek használata a részecskék keletkezésének elkerülésére (pl. fiolák dugója)
- olyan termékek használata, amelyek nem törnek apró darabkákra felnyitásuk során (pl. műanyag tárolók használata, üvegampullák helyett)
- gyógyszer-inkompatibilitás elkerülése
3. ábra: Nyissa ki az ampullát vagy a fiolát a betegellátás szabályainak megfelelően. Az infúzió felszívásához használjon szűrős szálat.
A részecskeszennyeződés kockázata csökkenthető úgy, hogy a dolgozók gyógyszerbeadás előtt in line filterek és filtertűk segítségével szívják fel a gyógyszereket az üvegampullákból. Az in-line filter eszközök eltávolítják a:
- részecskeszennyeződést
- mikrobiológiai szennyeződést
- infúziós oldatban lévő levegőt
A legtöbb in-line filter alkalmas a törmelékek, a mikrobiológiai szennyeződések, valamint a levegőbuborékok hatékony eltávolítására:
- korai figyelmeztetésként szolgál
- biztosítja az infundátum optikai kontrollját
- megállítja az infúziót, amikor a szűrő eltömődik.
Ezen filterek használata azonban jelenleg még nem általánosan elterjedt. A szerelékrendszerben lévő szűrők a betegcsatlakozók közelében helyezhetők el.
Az in-line filterek használata az alábbiak szerint javasolt:
- Zsírokat nem tartalmazó oldatok esetében 0,2 mikrométeres filter használandó 14
- Zsírokat tartalmazó infúzióknál és a teljes parenterál táplálásra kész oldatok esetében 1,2 mikrométeres filter javasolt14
- Az ISO 8536-4 normája javasolja az infúziós szerelékekben elhelyezhető filterek használatát. Az általánosan használt filterek pórusmérete 15 mikrométeres ( ISO 8536-4)
A részecskeszennyeződés megelőzése céljából a British Pharmaceutical Nutrition Group az alábbi irányvonalakat adta meg.14,15
- Azokat az üveg ampullából kiszívott oldatokat, amelyeket a teljes parenterális tápszerhez keverünk, legalább 5 mikrométeres pórus méretű filteren át kell szívni. A filterrel ellátott tűk és adagoló tüskék szűrői hatékonyan csökkentik a részecskeszennyeződés kockázatát (3. ábra).
- Parenterális tápszerek adagolásakor mindig használjunk megfelelő pórusméretű filtereket (különös tekintettel a súlyos állapotú immunhiányos betegek, gyerekek, újszülöttek esetében, valamint az otthoni táplálásra szoruló betegeknél).
- Zsírtartalmú oldatok adagolására 1,2 mikrométeres filtereket alkalmazzunk (az előre kevert tápszerekhez is) és 24 óránként cseréljük őket.
Kiemelt biztonsági termékek
Tudományos bizonyíték
1 Werner BP, Winter G. (2015) Particle contamination of parenteralia and in-line filtration of proteinaceous drugs. Int J Pharm;496(2):250-67
2 Doessegger L, Mahler HC, Szczesny P, Rockstroh H, Kallmeyer G, Langenkamp A, Herrmann J, Famulare J. (2012) The potential clinical relevance of visible particles in parenteral drugs. J Pharm Sci; 101(8): 2635-44
3 Lee KR, Chae YJ, Cho SE, Chung SJ. (2011) A strategy for reducing particulate contamination on opening glass ampoules and development of evaluation methods for its application. Drug Dev Ind Pharm; 37(12): 1394-401
4 Lye ST, Hwang NC. (2003) Glass particle contamination: is it here to stay? Anaesthesia; 58(1): 93-4
5 Roth JV. (2007) How to enter a medication vial without coring. Anesth Analg; 104(6): 1615
6 Boehne M, Jack T, Köditz H, Seidemann K, Schmidt F, Abura M, Bertram H, Sasse M. (2013) In-line filtration minimizes organ dysfunction: new aspects from a prospective, randomized, controlled trial. BMC Pediatr; 13 : 21
7 Ortolani GA, Russell RL, Angelbeck JA, Schaffer J, Wenz B. (2004) Contamination control in nursing with filtration. Part 1: filters applied to intravenous fluids and point-of-use hospital water. J Infus Nurs; 27(2): 89-103
8 Anonymus [No authors listed]. (2004) Risks due to particles in infusion therapy--experts promote use of infusion filters. Krankenpfl J. 2004; 42(3-4): 97
9 Jack T, Boehne M, Brent BE, Hoy L, Köditz H, Wessel A, Sasse M. (2012) In-line filtration reduces severe complications and length of stay on pediatric intensive care unit: a prospective, randomized, controlled trial. Intensive Care Med; 38(6): 1008-1
10 Oie S, Kamiya A. (2005) Particulate and microbial contamination in in-use admixed parenteral nutrition solutions. Biol Pharm Bull; 28(12): 2268-70
11 Lehr HA, Brunner J, Rangoonwala R, Kirkpatrick CJ. (2002) Particulate matter contamination of intravenous antibiotics aggravates loss of functional capillary density in postischemic striated muscle. Am J Respir Crit Care Med; 165:514-520
http://www.ncbi.nlm.nih.gov/pubmed/11850345
12 Yorioka K, Oie S, Oomaki M, Imamura A, Kamiya A. (2006) Particulate and microbial contamination in in-use admixed intravenous infusions. Biol Pharm Bull;29(11):2321-3
http://www.ncbi.nlm.nih.gov/pubmed/17077539
13 Nassaji-Zavareh M, Ghorbani R. Peripheral intravenous catheter-related phlebitis and related risk factors. Singapore Med J. 2007 Aug;48(8):733-6
14 Ball PA. (2003) Intravenous in-line filters: filtering the evidence. Curr Opin Clin Nutr Metab Care; 6(3): 319-25
15 Bethune K Allwood M, Grainger C, Wormleighton C; British Pharmaceutical Nutrition Group Working Party. (2001) Use of filters during the preparation and administration of parenteral nutrition: position paper and guidelines prepared by a British pharmaceutical nutrition group working party. Nutrition;17(5):403-8
16 Gianino MM, Vallino A, Minniti D, Abbona F, Mineccia C, Silvaplana P and Zotti CM. A method to determine hospital costs associated with nosocomial infections (transl). Ann Ig 2007; 19(4): 381-92
http://www.ncbi.nlm.nih.gov/pubmed/17937330
17 Kossovsky N, Cole P, Zackson DA. Giant cell myocarditis associated with silicone. An unusual case of biomaterials pathology discovered at autopsy using X-ray energy spectroscopic techniques. Am J Clin Pathol 1990; 93(1): 148-52
http://www.ncbi.nlm.nih.gov/pubmed/2294695
18 Walpot H, Franke RP, Burchard WG, Agtermkamp C, Müller FG, Mittermayer C, Kalff G. The filter effectiveness of common 15-micron filters (DIN 58362). II: Scanning electron microscopy and roentgen analysis. Infusionstherapie 1989; 16(3): 133-9
http://www.ncbi.nlm.nih.gov/pubmed/2503453
19 Preston ST, Hegadoren K. Glass contamination in parenterally administered medication. J Adv Nurs 2004; 48(3): 266-70